Neue Methode entschlüsselt Rolle von Gen-Spleißen bei Krebs
Ein internationales Forschungsteam mit Schwerpunkt in Barcelona, Spanien, hat eine neue Methode entwickelt, mit der sich die Aktivität von Spleißfaktoren – zentralen Regulatoren der Genverarbeitung – deutlich präziser bestimmen lässt. Die Technik liefert neue Einblicke, wie Tumorzellen genetische Informationen verändern, um Wachstum, Immunflucht oder Therapieresistenz zu fördern. Die Ergebnisse wurden in der Fachzeitschrift Nature Communications veröffentlicht.
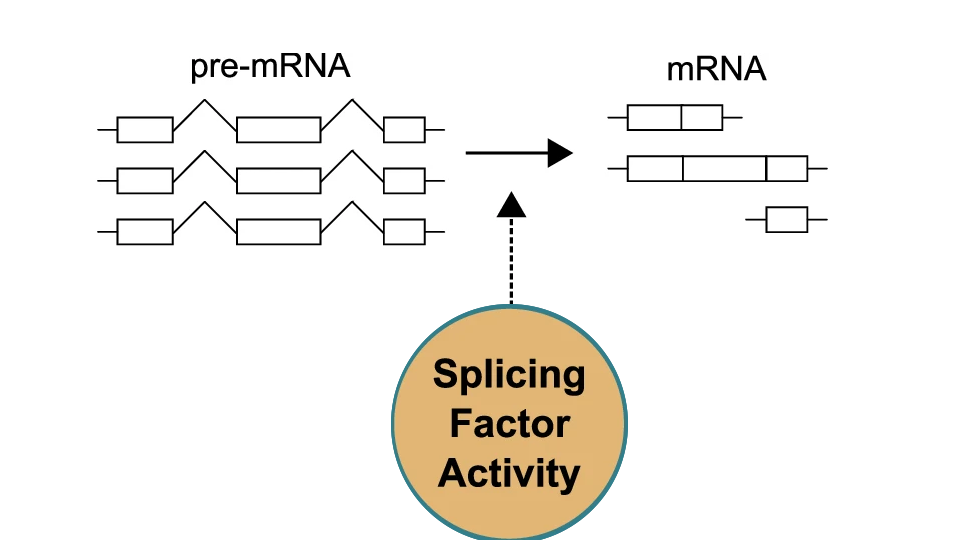
Beim sogenannten alternativen Spleißen werden aus einer Vorläufer-RNA unterschiedliche Varianten von Boten-RNA (mRNA) erzeugt. Dadurch kann ein einzelnes Gen mehrere verschiedene Proteine hervorbringen. Dieser Prozess wird von Spleißfaktoren gesteuert, deren Aktivität von zahlreichen molekularen Mechanismen beeinflusst wird – etwa durch Genexpression, Proteinmodifikationen oder ihre Position in der Zelle. Bisherige Analysen konzentrierten sich häufig nur auf einzelne dieser Faktoren und lieferten daher ein unvollständiges Bild.
Das Team um Miquel Anglada-Girotto vom Centre for Genomic Regulation in Barcelona und Kollegen der Columbia University wählte einen anderen Ansatz, der nun in Nature publiziert wurde: Statt die Spleißfaktoren selbst zu messen, analysierten sie direkt die Veränderungen bei der Einbindung einzelner RNA-Abschnitte, den sogenannten Exons. Diese „Exon-Inklusionssignaturen“ dienen als indirekter Hinweis darauf, wie aktiv bestimmte Spleißfaktoren tatsächlich sind.
Spleißen schafft Diversität, gibt aber auch eine Richtung vor
Für die Auswertung nutzten die Forscher eine angepasste Version des bioinformatischen Verfahrens VIPER (Virtual Inference of Protein Activity by Enriched Regulon analysis). Die Methode kombiniert Netzwerke von Spleißfaktor-Exon-Interaktionen mit RNA-Sequenzierungsdaten und berechnet daraus einen Aktivitätswert für einzelne Spleißfaktoren. Da nur Transkriptomdaten benötigt werden, lässt sich der Ansatz auch auf bereits vorhandene Datensätze anwenden.
Als Demonstration analysierte das Team rund 10.000 Tumorbiopsien aus 14 Krebsarten aus der Datenbank The Cancer Genome Atlas (TCGA). Dabei identifizierten die Forscher zwei grundlegende Spleißprogramme, die in vielen unterschiedlichen Krebsarten auftreten. Diese Programme stehen in Zusammenhang mit zentralen Eigenschaften von Tumoren wie Zellwachstum, Krankheitsentstehung und der Fähigkeit, dem Immunsystem zu entgehen.
FUS beeinflusst Spleißen – neues Zielmolekül?
Die Analyse deutet zudem auf etwa 120 Moleküle hin, die diese Spleißprogramme beeinflussen und damit potenzielle therapeutische Angriffspunkte darstellen könnten. Zu den auffälligen Kandidaten gehört das Gen FUS, das bislang vor allem mit neurodegenerativen Erkrankungen wie amyotropher Lateralsklerose in Verbindung gebracht wurde, aber offenbar auch eine Rolle bei bestimmten Krebsarten spielen könnte.
Nach Ansicht der Autoren könnte der Ansatz künftig nicht nur in der Krebsforschung, sondern auch bei anderen Krankheiten mit veränderten Spleißmustern eingesetzt werden – etwa bei neurologischen oder immunologischen Erkrankungen. Entscheidend ist dabei, dass die Methode komplexe regulatorische Einflüsse in einem einzigen Aktivitätssignal zusammenführt und so ein umfassenderes Bild der Genregulation ermöglicht.

 immatics GmbH / Max Lautenschläger
immatics GmbH / Max Lautenschläger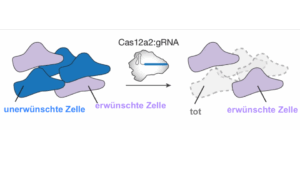 Scholz et al. https://www.nature.com/articles/s41586-026-10466-y/figures/4
Scholz et al. https://www.nature.com/articles/s41586-026-10466-y/figures/4 Biontech SE
Biontech SE